特应性皮炎(Atopic Dermatitis, AD)是一类典型的慢性炎症性皮肤疾病,其核心病理特征是Th2免疫反应异常激活与IgE水平显著升高。长期以来,AD研究多聚焦于皮肤屏障损伤与局部免疫紊乱;但近年来,“肠-皮轴(gut-skin axis)”成为前沿热点,越来越多证据表明:肠道菌群不仅影响肠道局部环境,还能够通过代谢物参与远端器官的炎症调控。
然而,一个关键的科学问题仍未被清晰解答:肠道菌群究竟通过何种分子机制影响Th2免疫,进而加重特应性皮炎?
近期,南方医科大学研究团队在Cell子刊《Immunity》(IF:26.3)上发表重磅研究,系统揭示了肠道免疫、菌群代谢与Th2炎症之间的关键联系。研究发现,肠道上皮TLR4缺失会引发菌群结构失衡,增强胆碱代谢并促使关键代谢物TMAO大量积累;升高的TMAO则进一步通过PPP5–PPARγ信号轴促进Th2细胞分化,最终加速AD进展。

该研究构建了完整的 “肠道菌群—代谢物—免疫炎症” 调控通路,为特应性皮炎及其他Th2相关疾病提供了全新机制解释与潜在干预方向。赛索飞生物为该研究提供了专业的基因合成服务,并交付高品质质粒,助力研究团队顺利完成关键实验与机制验证。
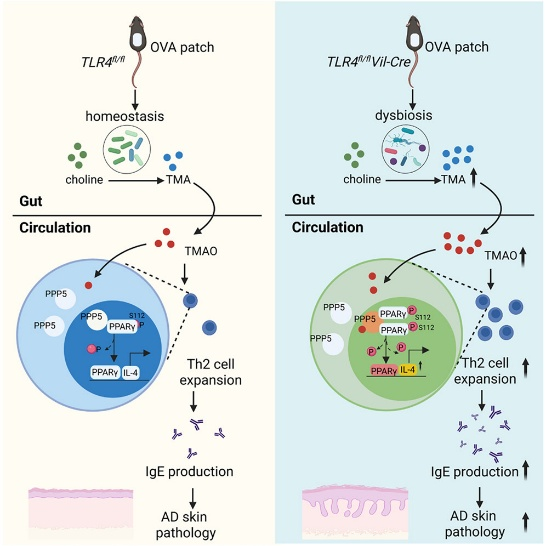
图1. 基于这一研究思路,研究团队首先构建了肠上皮特异性TLR4缺失模型,并结合菌群测序、代谢组学分析以及免疫功能实验,逐步解析肠道菌群与Th2炎症之间的调控机制。
研究思路:
靶向肠道免疫,挖掘AD调控新机制
TLR4是肠道上皮细胞中的重要模式识别受体,在维持肠道免疫稳态中发挥核心作用。研究团队提出科学假设:肠道TLR4异常可能影响菌群组成及代谢状态,进而调控系统性免疫反应,并参与AD进展。
为验证该假设,研究构建了肠上皮特异性TLR4缺失小鼠(TLR4fl/flVil-Cre),并分别在OVA诱导和MC903诱导的经典AD模型中观察疾病表型变化。结果显示,与对照组相比,TLR4缺失小鼠皮肤增厚更显著、炎症评分更高、抓挠行为更剧烈,同时血清IgE水平显著上升。
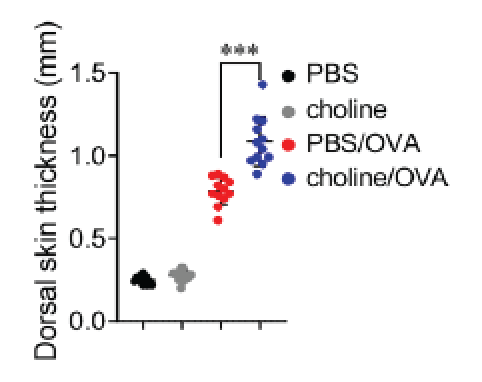
图2. TLR4缺失小鼠表现出更明显的皮肤炎症,疾病评分升高。
进一步实验证实,使用抗生素清除肠道菌群后,两组之间的炎症差异几乎完全消失。这一结果提示:TLR4对AD的调控并非仅来源于局部免疫,而是高度依赖肠道菌群的参与。
菌群重塑:
失衡微生态,触发胆碱代谢重编程
在明确肠道菌群的核心作用后,研究团队进一步对菌群结构和代谢变化进行分析。通过16S rRNA测序和宏基因组分析发现:TLR4缺失导致肠道微生态发生显著改变,其中有益菌Akkermansia muciniphila明显减少,而表达CutC酶、参与胆碱代谢的菌群则显著增加。
菌群的变化重塑了胆碱代谢通路:肠道菌群可将胆碱转化为TMA(trimethylamine),随后在体内进一步代谢生成TMAO(trimethylamine N-oxide)。研究显示,TLR4的缺失导致小鼠血浆中TMAO水平显著升高。
为了评估这一发现的临床相关性,研究团队还检测了AD患者血浆样本。结果表明,患者体内的TMAO水平明显高于健康人群,且与疾病严重程度(SCORAD评分)、IgE水平呈正相关。
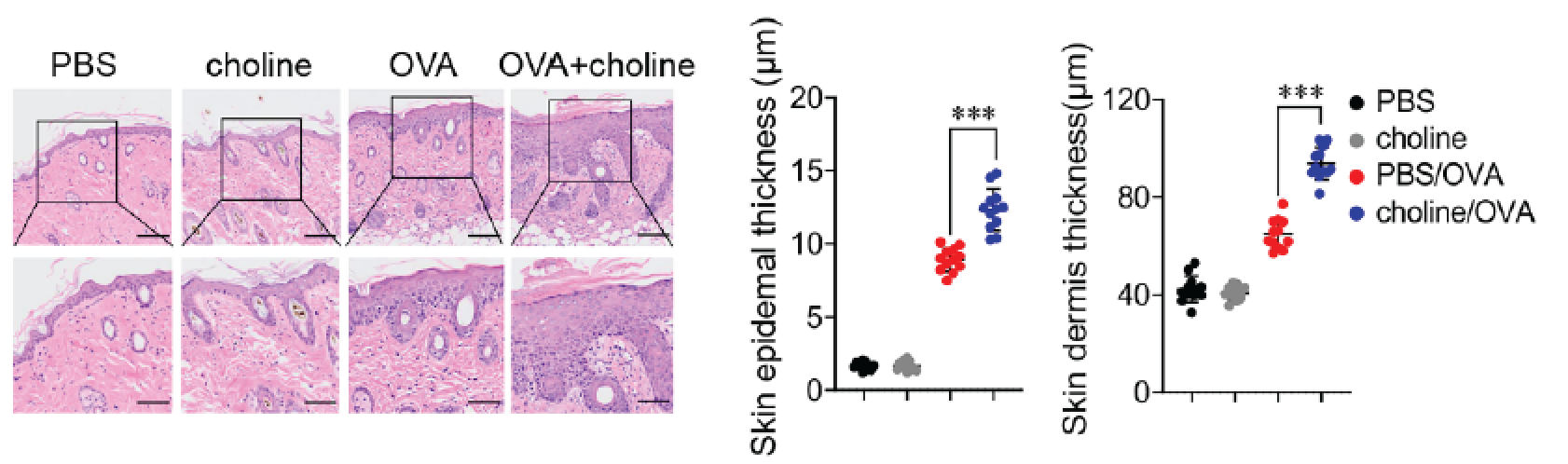
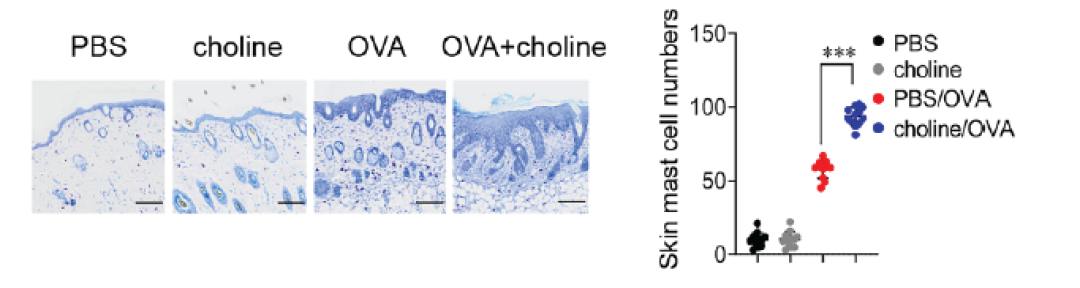
图3. AD患者体内TMAO水平显著升高,并与疾病严重程度呈正相关。
这些结果充分证实:TMAO是连接“肠道菌群变化”与“系统性炎症反应”的关键代谢介质。
机制解析:
关键代谢物TMAO,驱动Th2炎症反应
在发现TMAO水平异常升高后,研究团队进一步探索其对免疫反应的具体影响。
体外实验显示,在Th2极化条件下加入TMAO,可显著促进CD4+ T细胞向Th2方向分化,并增强IL-4、IL-5和IL-13等典型Th2细胞因子的表达。
在动物实验中,TMAO同样能够提高淋巴结中Th2细胞比例,并进一步加重皮肤炎症表现。当研究人员使用抗IL-4抗体进行干预后,这种促炎效应被明显削弱,说明TMAO主要通过经典Th2免疫通路发挥作用。
随后,研究进一步通过PPARγ功能干预实验,验证了这一通路的重要作用。在CD4+ T细胞中敲除PPARγ后,TMAO对Th2分化及IL-4表达的促进作用显著减弱,证实了PPP5–PPARγ信号轴在Th2炎症调控中的关键作用。
为进一步解析PPP5在该过程中的具体作用机制,研究人员构建了PPP5不同功能结构域,并对TMAO与PPP5之间的结合区域进行了分析。结果显示,TMAO能够与PPP5特定结构域发生结合,从而促进PPP5–PPARγ复合物形成并增强PPARγ去磷酸化,进一步揭示了TMAO调控Th2炎症反应的分子机制。
图4. 研究进一步通过PPP5结构域功能分析,揭示了TMAO促进PPP5–PPARγ信号激活的分子机制。
研究总结:
“肠-皮轴”新通路,点亮疾病干预新方向
本研究系统构建出一条完整的“肠-代谢-免疫-皮肤”调控通路:
肠道TLR4缺失 → 菌群结构改变 → 胆碱代谢增强 → TMAO升高 → PPP5激活 → PPARγ信号增强 → Th2分化 → 皮肤炎症加重
这一研究不仅进一步完善了“肠-皮轴”的理论框架,也揭示了微生物代谢物在Th2炎症调控中的重要作用。未来,针对肠道菌群、胆碱代谢、PPP5–PPARγ信号轴的干预策略,有望为特应性皮炎、哮喘等Th2相关疾病提供全新治疗思路。
赛索飞生物为本研究提供高品质基因合成与质粒构建服务,以精准序列、稳定交付与严格质控,确保实验体系高效稳定、研究数据真实可靠,助力科研成果快速突破与落地。



